La energía electrónica de un estado sólido de material se refiere a los niveles de energía de los electrones en un material sólido. Estos niveles de energía están determinados por las bandas de energía en el material. Las bandas de energía son rangos de energía con muchos niveles de energía permitidos adyacentes, muy cercanos entre sí. En un elemento particular, la magnitud de la influencia de los átomos vecinos depende del espaciado y la ubicación del electrón dentro del grupo de átomos. Cuando otros átomos están cerca, los niveles de energía electrónica discretos de los átomos individuales se convierten en bandas de energía.
La banda de valencia comprende los electrones de mayor energía en el sólido, y la banda de conducción es la banda vacía más baja donde los electrones pueden permanecer. Estas bandas son las bandas permitidas. La banda de energía entre las bandas permitidas es la banda prohibida o brecha de energía, donde los electrones no pueden existir. Las energías dentro de la banda prohibida no son accesibles para la ocupación electrónica. La energía de la banda prohibida es la diferencia entre las bandas de valencia y conducción.
Las propiedades eléctricas de un sólido dependen en gran medida del número de electrones en la banda de valencia. Los niveles de energía atómica se comparan con las bandas de energía en un material sólido mediante la estructura de bandas de energía de electrones.
Estructura de bandas de energía en sólidos
Un electrón en un átomo ocupa uno de una serie de patrones de orbital permitidos, con energías expresamente permitidas. En un cristal excitado, un electrón se eleva de un orbital de valencia a un orbital superior excitado. Existe una diferencia de energía entre el nivel de energía de valencia más alto y el nivel de energía orbital excitado más bajo: la brecha de energía.

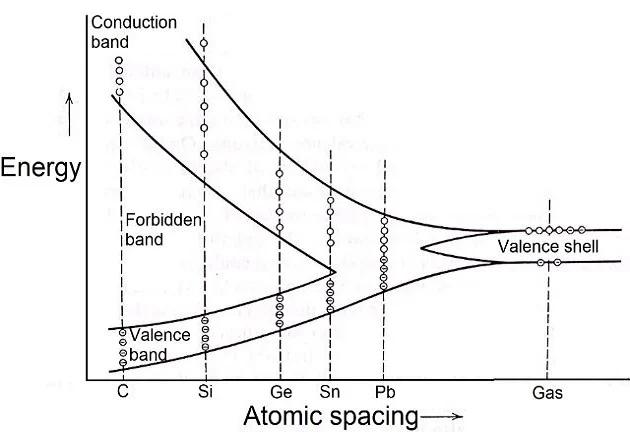
La banda de energía se forma cuando el espaciado de la red disminuye desde su valor inicial. A medida que se reduce el espaciado, la banda se divide en diferentes bandas de valencia y conducción con una brecha de energía en el medio. Cada banda contiene tantos niveles discretos de energía como átomos en el cristal.
Estructura electrónica de los sólidos en química de estado sólido
La energía electrónica es de hecho un valor propio del hamiltoniano electrónico y no incluye la contribución de las repulsiones de los núcleos fijos. Sin embargo, a veces el término energía electrónica se utiliza incorrectamente para referirse a la energía total para una configuración nuclear particular (que incluye la contribución de las interacciones mencionadas anteriormente), mientras que solo un valor propio del hamiltoniano electrónico se llama energía electrónica pura.
En cuanto a las estructuras de bandas de energía en sólidos, los programas de estructura electrónica citan la energía total como la energía electrónica. Sin embargo, esto no es cierto para todos los programas, ya que algunos programas citan correctamente los componentes de energía relacionados con las interacciones de los núcleos fijos.
La energía electrónica de un estado sólido de material se refiere a los niveles de energía de los electrones en un material sólido, que están determinados por las bandas de energía en el material. Estas bandas de energía representan una serie de niveles discretos de energía en un átomo individual y pueden dividirse en bandas de valencia y conducción con una brecha de energía en el medio. La energía electrónica de un estado sólido de material es un concepto fundamental en la química de estado sólido y es crucial para comprender las propiedades eléctricas y electrónicas de los materiales sólidos.